デ・ウエスタン・セラピテクス研究所の平均年収
デ・ウエスタン・セラピテクス研究所とは
| 企業名 | デ・ウエスタン・セラピテクス研究所 |
|---|---|
| 本社所在地 | 名古屋市中区錦一丁目18番11号 |
| 売上高 | 4.12億円 |
| 社員数 | 17人 |
| 平均年収 | 610万円 |
| 推定初任給 | 26万円 |
| 年収偏差値 | 57.1 |
| 平均年齢 | 46.4歳 |
| 平均勤続年数 | 10.4年 |
有価証券報告書によるとデ・ウエスタン・セラピテクス研究所の事業内容は次の通りです。
当社グループは、当社及び連結子会社日本革新創薬株式会社(以下、「JIT」)の2社で構成されており、プロテインキナーゼ(*)阻害剤(*)を中心とした医薬品の研究開発を行い、開発品を製薬会社等にライセンスアウトすることによって収益を獲得する創薬事業を展開しております。
当社グループ事業の系統図は以下のとおりです。
(1)創薬事業について
① 新薬開発の流れ
一般的に新薬の開発に際しては、基礎研究、非臨床試験、臨床試験、厚生労働省(あるいはアメリカ食品医薬品局(FDA)等の各国の医薬品許認可審査機関)への製造(輸入)承認申請、医薬品としての承認取得、薬価申請・収載を経て販売が開始され、患者様へ提供することが可能となります。このうち基礎研究活動は、新薬候補化合物の合成、スクリーニング(*)、スクリーニング毒性(*)の手続により実施されます。前述の基礎研究活動が終了した後、人に対する臨床試験の前に医薬品として満たすべき条件を、実験動物を用いて副作用及び安全性、安定性の検証を行う非臨床試験によって検証します。その後の臨床試験は、第Ⅰ相臨床試験、第Ⅱ相臨床試験、第Ⅲ相臨床試験の段階をもって実施されます。(下図参照)
② 創薬事業の概要
通常、新薬の研究開発過程において、非臨床試験から臨床試験へと開発が進捗するにしたがって、開発コストは大幅に増加し、また一定規模以上の自社臨床開発体制が必要となります。
当社グループは、研究開発活動の結果として、比較的早期の開発段階において開発品を製薬会社等へライセンスアウトしておりますが、これにより、臨床開発の推進に強みを持つ製薬会社等が開発を行うこととなり、自社での開発を継続する場合に比べて、低コストでの開発体制を維持できます。
このように、当社グループの創薬事業の特徴は、一般的な医薬候補品を開発するベンチャー企業に比べ、比較的早期の研究開発段階においてライセンスアウトが達成される点にありますが、これは、当社グループが基礎研究推進における独自の技術力を有していることと、その技術を基礎研究段階において十分に活用することにより効率的な研究開発が行われていることが要因と考えております。
当社グループの売上高は、主にライセンスアウト時に受領するフロントマネー収入、臨床開発進行に伴いその節目毎に受領するマイルストーン収入、製品上市(*)後販売額の一定比率を受領するロイヤリティ収入等によるものです。既に「リパスジル塩酸塩水和物(グラナテック®点眼液0.4%(以下、「グラナテック」)、グラアルファ®配合点眼液(以下、「グラアルファ」)及び「K-321」)」、「K-134」、「DW-1002」及び「DW-1001」はいずれも製薬会社にライセンスアウト済みであり、「グラナテック」、「グラアルファ」及び「DW-1002(欧州・米国等)」については、上市されロイヤリティ収入を得ております。これらのフロントマネー収入、マイルストーン収入、ロイヤリティ収入等を新規開発プロジェクトに投入することによって、次なる新規開発品の開発を進めております。
当社グループの主な売上高は、以下のもので構成されております。
売上高 | 内容 |
フロントマネー収入 | ライセンスアウト時に受領する収入。契約締結時に発生するため、契約一時金とも言う。 |
マイルストーン収入 | 臨床開発進行に伴いその節目毎に受領する収入。 |
ロイヤリティ収入 | 製品上市後販売額の一定比率を受領する収入。特許を実施する際に得られる収入のため実施料、ライセンス料とも言う。 |
③ 開発パイプラインについて
現在、当社グループが保有する開発パイプラインは以下のとおりです。
開発コード等 | 対象疾患 | 開発段階 | 地域 | ライセンスアウト先 | |
リパスジル 塩酸塩水和物 | グラナテック | 緑内障・高眼圧症(*) | 上市 | 日本、アジア(注1) | 興和 |
K-321 | フックス角膜内皮変性症(*) | 第Ⅲ相臨床試験 | 米国 | ||
リパスジル塩酸塩水和物/ブリモニジン酒石酸塩 | グラアルファ | 緑内障・高眼圧症 | 上市 | 日本 | |
DW-1002 | 内境界膜染色 | 上市 | 欧州・米国等 | DORC | |
第Ⅲ相臨床試験 | 日本 | わかもと製薬 (WP-1108) | |||
水晶体前嚢染色(*) | 第Ⅲ相臨床試験 | 日本 | |||
DW-1001 | 眼科用治療剤 (非開示) | 第Ⅰ相臨床試験 | 日本 | ロート製薬 | |
K-134(注2) | ― | ― | 日本 | 興和 | |
H-1337 | 緑内障・高眼圧症 | 後期第Ⅱ相臨床試験 | 米国 | 自社開発 | |
DW-5LBT | 帯状疱疹後の神経疼痛 | 申請 | 米国 | メドレックスと共同開発(MRX-5LBT) | |
DWR-2206 | 水疱性角膜症 | 非臨床試験 | 日本 | アクチュアライズと共同開発(AE101) | |
未熟児網膜症(*)治療薬 (注3) | 未熟児網膜症 | 臨床試験準備中 | 日本 | 子会社JIT開発 | |
(注1)アジア一部地域において上市されております。
(注2)ライセンスアウト先の興和により、閉塞性動脈硬化症(*)以外の適応症への応用を検討されているため、対象疾患と開発段階は記載しておりません。
(注3)JITは未熟児網膜症等診断薬について、アジア一部地域における独占的実施権をSplendor Health International Limitedに再許諾するライセンス契約を締結しております。
各開発パイプラインの詳細は以下のとおりです。
(イ)リパスジル塩酸塩水和物
(a)グラナテックⓇ点眼液0.4%(対象疾患:緑内障・高眼圧症)
本開発品は、プロテインキナーゼ(*)の一種であるRhoキナーゼ(*)を選択的に阻害するイソキノリンスルホンアミド化合物(*)であり、眼圧下降作用により緑内障・高眼圧症を治療する点眼剤です。緑内障治療剤における世界初の作用機序(*)を有しており、Rhoキナーゼを阻害することにより、線維柱帯-シュレム管を介する主流出路からの房水流出を促進することで眼圧を下降させます。
当社は、2002年に本開発品の全世界の権利を興和株式会社(以下、「興和」)にライセンスアウトいたしました。その後は興和により臨床試験が進められ、2014年に緑内障・高眼圧症を適応症として国内上市されました。さらに、海外展開も進められ、アジア一部地域において承認取得、販売開始されております。
(b)K-321(対象疾患:フックス角膜内皮変性症)
Rhoキナーゼ阻害剤(*)であるグラナテックは、眼内にあるキナーゼに作用する可能性があることが示唆されており、他眼科疾患への適応可能性が検討されておりました。適応拡大に向けた取り組みとして、2019年に米国第Ⅱ相臨床試験のIND申請(治験許可申請)がなされ、興和にてフックス角膜内皮変性症を適応症とした試験が進められ、その後、2022年8月に米国第Ⅲ相臨床試験が開始されました。フックス角膜内皮変性症の治療法は角膜移植しか存在しないのが現状であり、有効な治療薬の開発が望まれています。
(c)グラアルファⓇ配合点眼液(対象疾患:緑内障・高眼圧症)
本開発品は、リパスジル塩酸塩水和物とブリモニジン酒石酸塩を含有する世界で初めての組み合わせの配合点眼剤です。2020年より、興和にて緑内障・高眼圧症を適応症として国内第Ⅲ相臨床試験が行われ、2022年12月に国内上市されました。緑内障の治療は、多剤併用が標準的な治療法となりつつあります。本開発品により、アドヒアランスの向上が期待され、緑内障患者様の治療に貢献できるものと考えております。
(ロ)DW-1002(対象疾患:内境界膜染色、水晶体前嚢染色)
本開発品は、国立大学法人九州大学の研究グループが発見したBBG250(Brilliant Blue G-250)という染色性の高い色素を主成分とした眼科手術補助剤について、独占的ライセンスに基づき開発している開発品で、眼内にある内境界膜又は水晶体を保護するカプセルを一時的に安全に染色し、硝子体・白内障(*)の手術を行いやすくするものです。当社は、2017年に本事業を譲受いたしました。
日本以外の全世界向けの独占的なサブライセンスをDutch Ophthalmic Research Center International B.V.(以下、「DORC」)に付与しており、DORCは硝子体手術時の内境界膜染色を対象として、2010年から欧州等において、この眼科手術補助剤を製造・販売しております。2020年には米国においても販売開始し、現在は、欧州・米国を含む世界76の国と地域で販売されております。
国内については、わかもと製薬株式会社(以下、「わかもと製薬」)に独占的サブライセンスを付与しており、わかもと製薬は硝子体手術時の内境界膜染色、白内障手術時の水晶体前嚢染色を対象として、製造販売承認取得に向けて開発を進めております。
(ハ)DW-1001(対象疾患:非開示)
本開発品は、2015年に英国企業から導入した眼科用治療剤です。
他の疾患を適応症として既に市販されている化合物を眼科適応への適応拡大を目指す、いわゆるリポジショニングの手法での開発を目指しており、開発のコスト並びにリスクは相対的に低くなることが期待されます。
2019年に日本における独占的実施権をロート製薬株式会社(以下、「ロート製薬」)にライセンスアウトいたしました。ロート製薬では、非臨床試験を進め、2022年3月に国内第Ⅰ相臨床試験を開始し、12月に良好な結果で終了いたしました。現在、国内第Ⅱ相臨床試験の準備が進められております。
(ニ)K-134(対象疾患:検討中)
本開発品は、1993年より当社創業者と大塚製薬株式会社(以下、「大塚製薬」)の共同研究により、血管内膜肥厚抑制作用(*)を併せ持つ抗血小板剤(*)として開発が開始されました。
本開発品の全世界での権利は、2002年に大塚製薬より当社へ全て譲渡され、当社は同年に全世界の権利を興和にライセンスアウトしました。その後は興和により、閉塞性動脈硬化症に伴う間歇性跛行(*)症状を対象疾患として開発が行われておりましたが、2014年に終了した国内後期第Ⅱ相臨床試験の結果を総合的に検討した結果、閉塞性動脈硬化症を適応症とした開発は中止されました。他適応症への応用につきましては、興和にて検討されております。
(ホ)H-1337(対象疾患:緑内障・高眼圧症)
本開発品は、プロテインキナーゼ阻害剤を中心とする当社化合物ライブラリー(*)のシード化合物を基にして最適化された、緑内障・高眼圧症を対象疾患とする開発品です。当社初となる自社臨床開発を行っており、2018年に米国第Ⅰ相/前期第Ⅱ相臨床試験を終了いたしました。試験結果は良好で、有効性の主要評価項目で本開発品の有効性が確認され、安全性に関して重篤な有害事象は認められませんでした。2022年12月に、米国後期第Ⅱ相臨床試験の治験届を提出いたしました。
また、適応拡大の研究を進めており、滲出型加齢黄斑変性に対する治療効果、並びに肺高血圧に対する治療効果も動物試験において確認されております。
(ヘ)DW-5LBT(対象疾患:帯状疱疹後の神経疼痛)
本開発品は、イオン液体を利用した株式会社メドレックス(以下、「メドレックス」)の独自技術ILTS(Ionic Liquid Transdermal System)を用いた新規のリドカイン(*)テープ剤であり、リドカインパップ剤Lidodermの市場をターゲットとして開発が進められております。メドレックスが帯状疱疹後の神経疼痛治療薬として開発を進めており、当社は2020年に共同開発を開始いたしました。2020年に米国FDA(米国食品医薬品局)に承認申請いたしましたが、2021年に審査完了報告通知を受領いたしました。承認取得のために必要であると指摘を受けた追加試験は良好な結果で終了しており、2023年前半に再申請する予定です。
(ト)DWR-2206(対象疾患:水疱性角膜症)
本開発品は、水疱性角膜症を適応症とした再生医療用細胞製品で、培養ヒト角膜内皮細胞とROCK阻害剤を含有した懸濁液を前房内に注入し、角膜内皮の再生の治療に用いられます。アクチュアライズ株式会社が開発を進めており、当社は2022年に共同開発を開始いたしました。当社初となる再生医療品であり、現在、国内臨床試験に向けた準備を進めております。
(チ)未熟児網膜症治療薬(対象疾患:未熟児網膜症)
本開発品は、国立大学法人東京農工大学及び東京バイオマーカー・イノベーション技術研究組合により見出され、未熟児網膜症発症の重要な原因であることが患者様で確認されている蛋白質を阻害する化合物です。他の疾患を適応症として既に市販されている化合物を本適応症への適応拡大を目指す、いわゆるリポジショニングの手法での開発を目指しており、開発のコスト並びにリスクは相対的に低くなることが期待されます。
子会社JITが未熟児網膜症の診断薬に関する特許も含めて権利を有しており、2020年には、未熟児網膜症等診断薬に関する特許について、アジア一部地域(中華人民共和国、香港行政特別エリア、台湾地域)における独占的実施権を、Splendor Health International Limitedに再許諾するライセンス契約を締結いたしました。
④ 研究プロジェクトについて
当社グループは、プロテインキナーゼ阻害剤を中心とした新薬候補化合物の創出を行っております。プロテインキナーゼを対象とする疾患は様々ですが、特に眼科関連疾患に注力した研究を推進しております。また、自社の創薬基盤技術を活かし、他社との提携を積極的に推進しております。
主なプロジェクトとしては、眼科関連疾患や神経系、呼吸器系疾患等を対象としたシグナル伝達阻害剤開発プロジェクトを当社開発研究所(国立大学法人三重大学の研究施設)において行っております。また、共同研究として、ユビエンス株式会社との標的タンパク質(*)分解誘導薬プロジェクト、SyntheticGestaltとの炎症系・中枢系疾患を対象にしたキナーゼ阻害剤のAI創薬プロジェクト等、複数のプロジェクトを進めております。
⑤ 創薬事業における当社グループ技術と研究開発の特徴について
創薬事業における当社グループ技術と研究開発の特徴は以下のとおりです。
(イ)プロテインキナーゼ阻害剤を中心とした新薬候補化合物の創製
当社グループは主にプロテインキナーゼ阻害剤を中心とした研究開発を進めております。
プロテインキナーゼは、細胞の分化、増殖等の細胞内情報伝達(*)機能を担っている重要な酵素であるとされており、そのプロテインキナーゼに対し、有望な新薬候補品である阻害剤を投与することによって治療効果を高めるのが当社グループの開発の特徴であります。
当社は、有望な新薬候補品を創製するために、独自に開発した化合物ライブラリーを保有しており、これらの開発過程で蓄積したデータやノウハウを活用して、新薬候補化合物を合成しておりますが、これらの技術力が高いことから有効な新薬候補化合物が見つかる可能性が高いと考えております。
(ロ)当社独自の標的タンパク質の同定(*)方法であるドラッグ・ウエスタン法(*)の活用
当社は、ドラッグ・ウエスタン法という独自に開発した方法を使って、新薬候補化合物の標的タンパク質を同定しております。生物学の分野では、標的タンパク質を同定するために様々な方法が利用されてきましたが、当社は、それらを踏まえて医薬品開発への応用を図り、ドラッグ・ウエスタン法を完成させました。
この方法の活用により、他の手法を活用した際に困難である新薬候補化合物の標的タンパク質の特定が容易になるほか、1回のスクリーニングで多数の標的タンパク質を同定することが可能です。既存の方法に対して、生物材料や化合物の消費量が少ないこと、スクリーニングの操作が単純であり短時間で完了すること等の長所を持ちます。
ドラッグ・ウエスタン法を活用した際の効果は、以下のとおりと考えられます。
a. 有効性:高い有効性を持つ新薬候補化合物の開発の可能性が高まります。新薬候補化合物の標的タンパク質を早期に同定することによって、その新薬候補化合物の作用機序が明らかになり、その結果から、有効な新薬候補化合物の開発へとつなげていくことが可能になると考えております。
b. 安全性:副作用や他の医薬品との相互作用の予測により、高い安全性を持つ新薬候補化合物の開発の可能性が高まります。早期に標的タンパク質を同定することによって、副作用が起こるメカニズムの推測もしやすくなり、それにより、安全性の高い新薬候補化合物の開発が可能となります。また、作用メカニズムが明らかになることにより、他の薬剤との併用の可能性の分析がしやすくなり、薬としての利用機会の拡大とリスクの低減につながりやすいと考えます。
既にこの方法を用いて、当社グループのパイプラインの「K-134」についても標的タンパク質が同定されました。
(ハ)細胞内情報伝達研究に由来する分子薬理学(*)に関する経験及びノウハウの活用
当社グループの創業者は、長年にわたって細胞内情報伝達の研究活動及び創薬活動に従事してきており、その研究・創薬活動の中で、これまでに製薬会社と共同で2つの上市薬の誕生に貢献しております。当社グループは、こうした活動において獲得した経験とノウハウを基盤に、研究開発活動を行い、2014年には当社設立以来初の上市薬が誕生いたしました。
当社グループの新薬の開発は、この分子薬理学に関する経験及びノウハウを駆使し、新薬候補化合物を設計し、合成することによって開始されております。ここで合成された新薬候補化合物の薬理学的傾向は、過去の分子薬理学に関する経験及びノウハウからある程度予測することが可能であるため、その予測を基に効率的な研究開発が可能になると考えております。
(ニ)提携関係を活用した研究開発体制
当社グループは、国立大学法人三重大学との産学官連携講座(後述「第一部 企業情報 第2 事業の状況 4 経営上の重要な契約等」参照)による共同研究等の提携関係を構築し、技術の取り込みを図り研究活動を進めております。また、研究開発の推進に向けては、業務受託企業等外部の企業を積極的に活用しております。こうした企業外部との提携関係を活用することによって、効率的な研究開発体制を構築することが可能となっております。
当社グループと外部機関との関係図(研究開発体制)
<用語解説>(アルファベット、あいうえお順)
* Rhoキナーゼ
タンパク質リン酸化(*)酵素(プロテインキナーゼ)の1つであり、Rho-ROCK経路を介する多彩な細胞応答の制御機構に関与する酵素です。
* イソキノリンスルホンアミド化合物
当社が開発している化合物の有する骨格(形)の名称です。
* 化合物ライブラリー
当社が長年にわたり蓄積してきた新薬候補化合物のタネとなる化合物群です。これらの化合物の一つ一つが特徴的な性質を有しており、基礎研究や新薬候補化合物発見に利用されます。
* 間歇性跛行
閉塞性動脈硬化症により引き起こされる典型的な症状です。一般に下肢筋肉への動脈血供給を妨げる閉塞性病変が原因となって血流障害が引き起こされ、歩行運動に伴って虚血性の疼痛を発生させます。この疼痛は一定の運動負荷で引き起こされ、安静により数分以内に緩和される特徴があります。跛行症状の治療には、下肢血行動態の改善を目的とした監視下運動療法、薬物療法及び血行再建術があります。
* 血管内膜肥厚抑制作用
血管内膜肥厚とは、血管壁の損傷により血管壁が厚くなることであり、その結果血液の流路が細くなり、血行障害が生じやすくなります。この血管内膜肥厚を抑制することは動脈硬化を防ぐためには重要であると考えられており、その抑制作用を血管内膜肥厚抑制作用と言います。
* 抗血小板剤
血小板(血液の成分の1つで血液の凝固や止血に重要な役割を果たしている成分)が有する機能の1つである凝集機能を阻害(抑制)する薬です。
* 細胞内情報伝達
神経刺激やホルモン等の細胞外からのシグナル(信号)を細胞内の必要な箇所へ伝えるシステムのことを言います。細胞内シグナル伝達とも言います。
* 作用機序
薬物が作用する仕組みのことを言います。近年では薬物作用の明確化の重要性が高まっており、この作用機序の解明が新薬開発において注目されております。
* 上市(じょうし)
新薬が承認され、実際に市場に出る(市販される)ことを言います。
* 水疱性角膜症
角膜内皮細胞が障害を受け、角膜浮腫が起こり、角膜が白く濁って視力が著しく低下する病気。フックス角膜内皮ジストロフィ、白内障や緑内障等の眼科手術により角膜内皮細胞が減少することが原因にあげられます。治療法は角膜移植手術になります。
* スクリーニング
新薬を開発するには、多数の候補化合物の中から、効果があり安全性が高いものを選び出すことが必要となります。このような多数の化合物から新薬の候補を探す一連の流れをスクリーニングと言います。
* スクリーニング毒性
細菌を用いる復帰突然変異試験(化学物質による、発癌性を含めた遺伝子に与える変化である変異原性を、細菌を用いてテストする試験)、ほ乳類培養細胞を用いる染色体異常試験(明確な染色体構造を持たない細菌においては、染色体異常を検出できないため、人為的に生体外で培養したほ乳動物の細胞を用いて、染色体に対する遺伝毒性がないかをテストする試験)及びほ乳類を用いる28日間の反復毒性試験(ラット等の動物に一定期間毎日反復投与したときに現れる生体機能及び形態の変化を観察する試験)によって検出される毒性を指します。
* 阻害剤
生体内の様々な酵素分子に結合して、その酵素の活性を低下もしくは消失させる物質を指します。化学物質が特定の酵素の活性を低下もしくは消失させることにより、病気の治療薬として利用されることがあります。
* タンパク質リン酸化
タンパク質にリン酸基を移転する化学反応であり、タンパク質の働きを調節すると考えられております。
* 同定
単離した化学物質等の標的が何であるかを決定することを指します。
* ドラッグ・ウエスタン法
薬物の標的タンパク質の同定に用いられる手法で、当社がバイオテクノロジーを応用して発明し、特許を有しておりました。煩雑なタンパク質精製プロセスを介さずに、薬物が結合する少量のタンパク質を検出し、その遺伝子を特定することにより標的タンパク質を同定することができる方法です。
* 白内障
水晶体が白く濁り、視力障害を引き起こす病気です。主な原因は加齢によるもので、症状が進行している場合には、濁った水晶体を取り除き、眼内レンズを挿入する手術が行われます。日本では年間およそ120万件の手術が行われています。
* 標的タンパク質
薬物が作用する対象となるタンパク質を標的タンパク質と呼びます。生体においては多くのタンパク質が相互に作用することによって様々な機能を果たしており、多くの病気が特定のタンパク質の異常な働きによって引き起こされております。これらの病気には、これらのタンパク質を標的タンパク質として、その異常な動きを抑制する薬剤が有効となりうると考えられております。
* フックス角膜内皮変性症
角膜内皮細胞に障害がおき、角膜浮腫・混濁が生じ、視力が低下していく疾患です。欧米で多くみられ、日本では患者数が少ないとされています。現在の治療法は角膜移植しか存在せず、有効な治療薬の開発が望まれています。
* プロテインキナーゼ
ATP(アデノシン三リン酸と言われ、体内で作られる高エネルギー化合物)等、生体においてエネルギーの元となる低分子物質等のリン酸基を、タンパク質分子に転移する(リン酸化)酵素です。一般にリン酸化を触媒する酵素をキナーゼと呼び、特にタンパク質をリン酸化するキナーゼをプロテインキナーゼと言います。
* 分子薬理学
薬理学とは、薬物が生体に対してどのような作用により、影響・効果を発揮しているかを調べたり、薬物を用いて生体の機能を明らかにしたりする学問のことです。分子薬理学とは、その薬理学の調査の対象を生物の化学的性質を失わない最小の構成単位、つまり遺伝子のレベルで調べる学問です。
* 閉塞性動脈硬化症
動脈硬化(動脈壁が肥厚し硬化した状態)により、主として下肢の大血管が慢性的に閉塞することによって、軽い場合には冷感、重症の場合には下肢の壊死にまで至ることがある病気を言います。軽度の場合には抗血小板剤が処方されることが多く、症状が悪化するにつれて他の薬剤を使用します。
* 未熟児網膜症
低出生体重児(未熟児)は、出生後保育器で高酸素下の環境におかれますが、その後通常の環境に戻された際、その環境に適応するため、急激に血管を産生しようと努めます。それは網膜においても起こり、急激な血管産生の結果、脆い異常な血管が形成されることで網膜剥離につながり、最終的には失明に至ることがある疾患です。現在は、レーザー照射による治療が行われていますが、必ずしも視力が戻るわけではなく、満足されている治療というわけではありません。
* リドカイン
神経末端において痛みの信号を遮断することにより痛みを軽減させる、局所麻酔薬の一種です。
* 緑内障・高眼圧症
緑内障とは、視神経と視野に特徴的変化を有し、通常、眼圧を十分に下降させることにより視神経障害を改善もしくは抑制しうる眼の機能的構造的異常を特徴とする疾患です。適切に治療されずに放置すると視野狭窄から失明に至る疾患であり、日本の中途失明原因の第一位(2005年)となっております。また、高眼圧症とは、視野狭窄が無いものの、眼圧が正常値を超えている病態です。
現在、緑内障のエビデンスに基づいた唯一確実な治療法は、「眼圧を下降すること」とされており、原発開放隅角緑内障(広義)に対する治療では、薬物治療が第1選択とされております。
デ・ウエスタン・セラピテクス研究所の平均年収は610万円
生涯収入の全国平均である約1.9億円に対し、デ・ウエスタン・セラピテクス研究所の生涯収入はおよそ2.26億円と推定されます。
| 年 | 平均年収 |
|---|---|
| 2013 | 422万円 |
| 2014 | 421万円 |
| 2015 | 433万円 |
| 2016 | 428万円 |
| 2017 | 489万円 |
| 2018 | 504万円 |
| 2019 | 493万円 |
| 2020 | 483万円 |
| 2021 | 573万円 |
| 2022 | 610万円 |
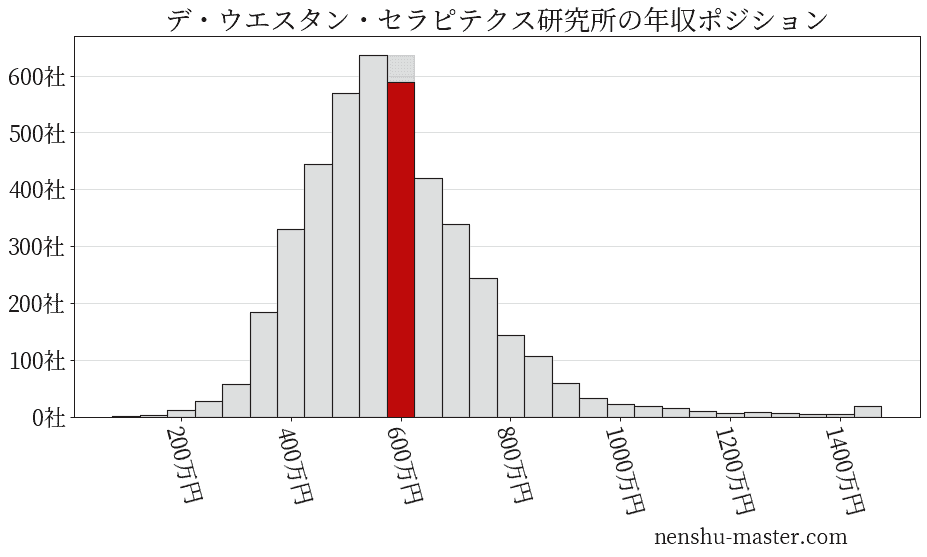
平均年収と社数のヒストグラム上ではデ・ウエスタン・セラピテクス研究所は赤色の箇所に位置しています。 年収ランキングではデ・ウエスタン・セラピテクス研究所は2232位(全4687社)で、年収偏差値は57.1でした。
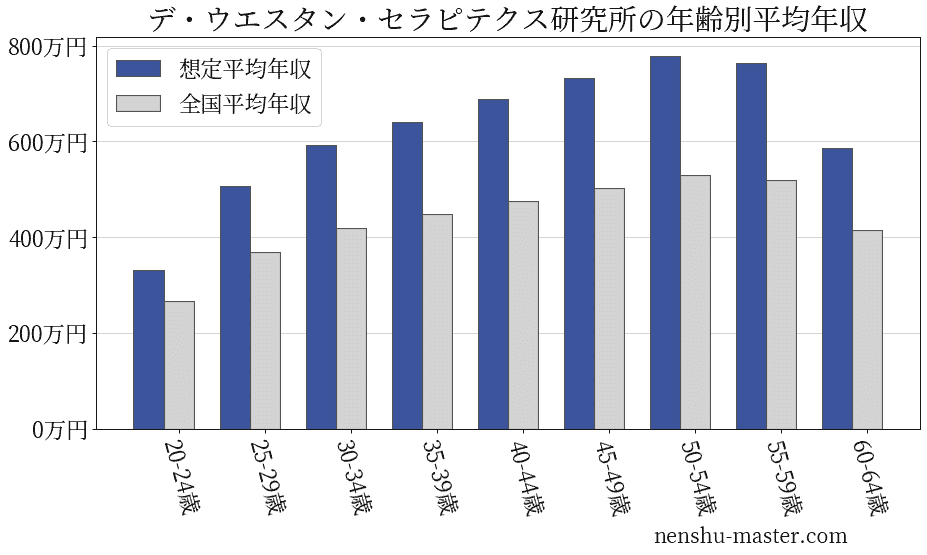
デ・ウエスタン・セラピテクス研究所の年齢別年収
| 年齢 | 想定平均年収 | 月額給与 |
|---|---|---|
| 20-24歳 | 332万円 | 26万円 |
| 25-29歳 | 507万円 | 39万円 |
| 30-34歳 | 593万円 | 46万円 |
| 35-39歳 | 641万円 | 49万円 |
| 40-44歳 | 688万円 | 53万円 |
| 45-49歳 | 733万円 | 56万円 |
| 50-54歳 | 779万円 | 60万円 |
| 55-59歳 | 763万円 | 59万円 |
| 60-64歳 | 586万円 | 45万円 |
デ・ウエスタン・セラピテクス研究所の賞与・ボーナス
| 年 | 平均賞与額 |
|---|---|
| 2013 | 56万円 |
| 2014 | 56万円 |
| 2015 | 58万円 |
| 2016 | 57万円 |
| 2017 | 65万円 |
| 2018 | 67万円 |
| 2019 | 66万円 |
| 2020 | 64万円 |
| 2021 | 76万円 |
| 2022 | 81万円 |
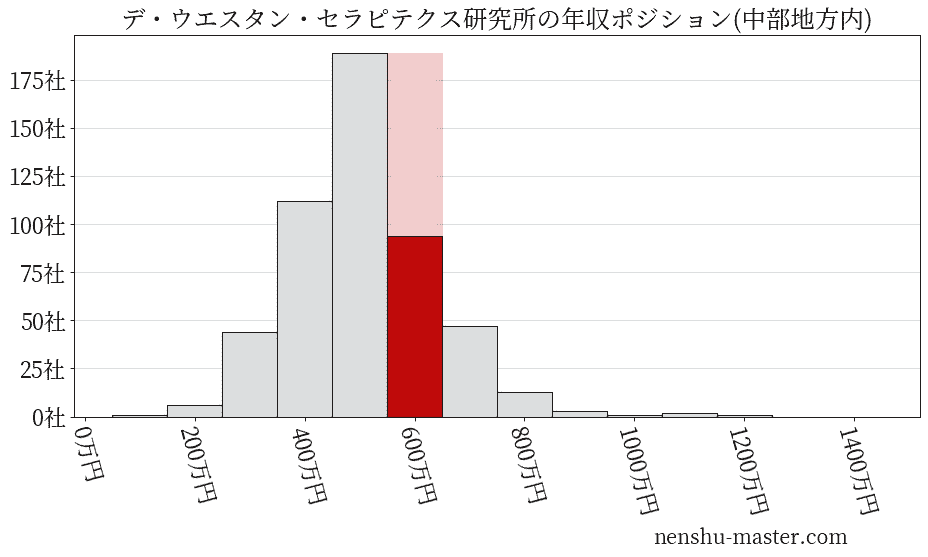
デ・ウエスタン・セラピテクス研究所の業種・地域
※こちらは、実際の企業数とは大きく異なる点に注意してください。多くの企業が本社所在地を東京にしているため、それ以外の地域では企業数が少なくなります。
医療・製薬業内での年収ランキング
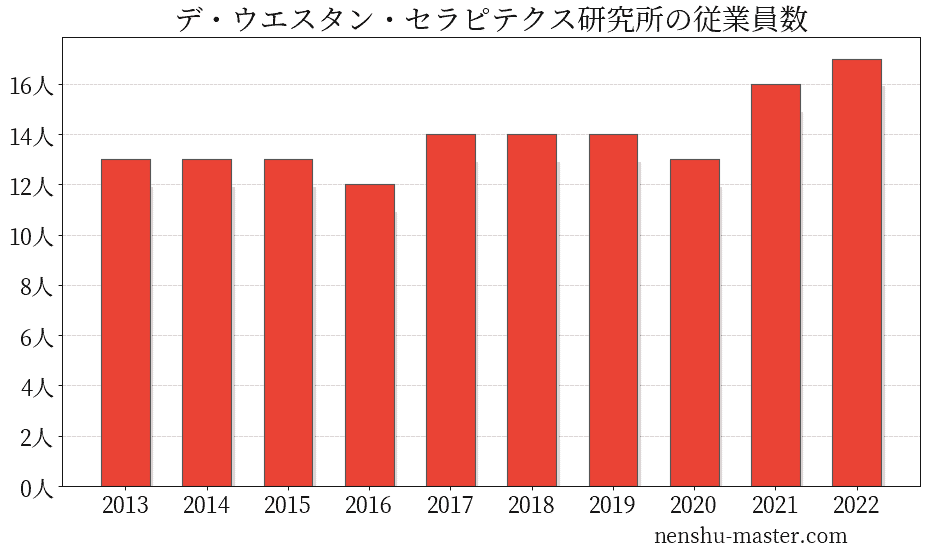
デ・ウエスタン・セラピテクス研究所の従業員数は17人
| 年 | 従業員数 |
|---|---|
| 2013 | 13人 |
| 2014 | 13人 |
| 2015 | 13人 |
| 2016 | 12人 |
| 2017 | 14人 |
| 2018 | 14人 |
| 2019 | 14人 |
| 2020 | 13人 |
| 2021 | 16人 |
| 2022 | 17人 |
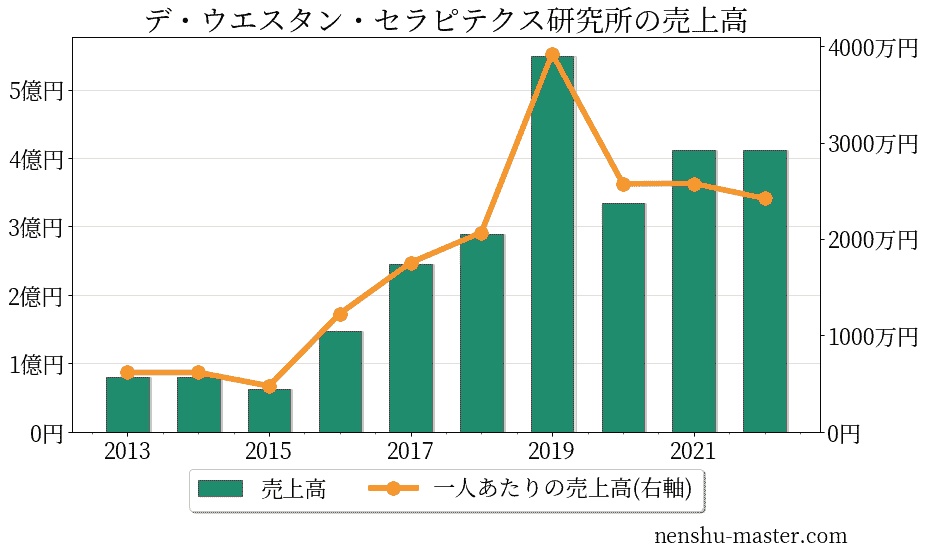
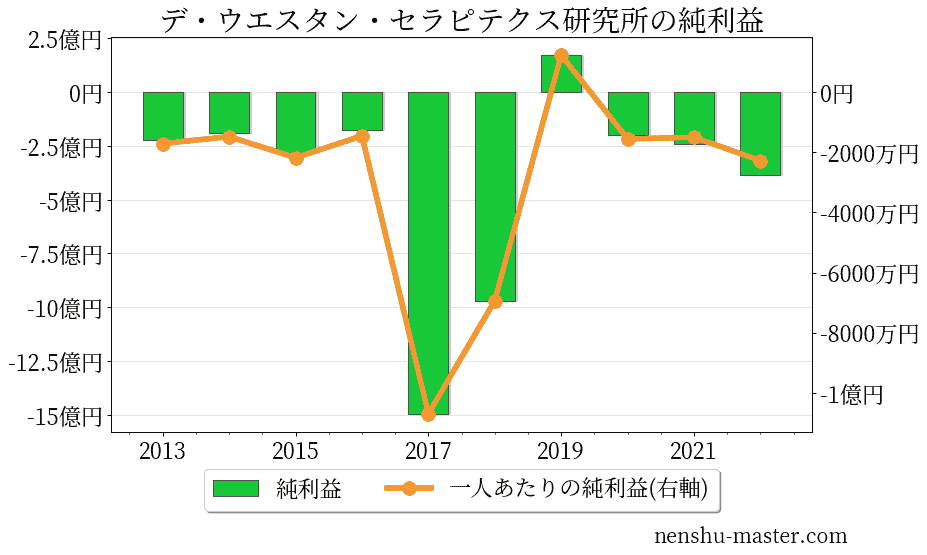
デ・ウエスタン・セラピテクス研究所の売上、純利益
【広告】デ・ウエスタン・セラピテクス研究所に転職するには?
転職サイトはサイトごとに特色があり、2〜3サイトを登録してそれぞれの良い部分を利用するのが賢い利用方法です。年収マスターイチオシのサイトを紹介します。
JACリクルートメント
「JACリクルートメント」はハイクラスな転職案件を多数持っており、市場価値の高い応募者におすすめのサイトです。 内資系の高額案件はもちろん、JACリクルートメントはイギリスやシンガポールでも展開しており、そのつながりを活かした外資系案件も多数あります。
他の転職サイトでは一気に大量の案件を提示されることがありどれを選べばわからないということが起こりますが、JACリクルートメントではそのようなことはありません。 ひとりの応募者につき複数のエージェントが担当し、選りすぐりの案件を紹介してくれるためマッチ度が高い仕事に出会えます。
ハイクラス案件をメインで扱うJACリクルートメントのみでしか得られない案件情報も多数あります。 上昇志向があり、現在のポジションからステップアップしてよりハイキャリアを目指す方にはイチオシのサイトです。
ランスタッド
「ランスタッド」は敏腕コンサルタントが専任で案件紹介をしてくれる転職サイトです。 ランスタッドのエージェントは評判が良く、最近人気が大きく伸びてきてきています。 よくある転職サイトはエージェントが十分なヒアリングも無くノルマ達成のためにたくさんの案件を紹介してきますが、 ランスタッドはそのようなことはありません。
ランスタッドは少数精鋭のコンサルタントで運営されており、現状のスキルや今後構築したいキャリアなどを入念にヒアリングした上で案件紹介をしてくれます。 特に20代後半から30代の転職に力を入れており、応募者にマッチした案件を紹介してくれます。
そのため案件の質も高く、JACリクルートメントと同様に高年収案件に強い印象です。800万円や1200万円を超える案件も多数あり、 ハイキャリアを目指す方には心強いパートナーです。ランスタッドのみでしか公開されてない案件もかなり多いので、 一度無料登録して相談してみることをオススメします。
参考書籍
デ・ウエスタン・セラピテクス研究所の歴史
| 1999年2月 | 医薬品研究開発を目的とした、有限会社デ・ウエスタン・セラピテクス研究所を愛知県名古屋市に設立 |
| 2006年12月 | 国立大学法人三重大学と産学官連携講座共同研究契約を締結し、同大学内に「臨床創薬研究学講座」を開設 |
| 2009年10月 | ジャスダック証券取引所NEOに株式上場 |
| 2018年3月 | H-1337の米国第Ⅰ相/前期第Ⅱ相臨床試験開始 |
| 2020年2月 | 緑内障治療剤の配合剤の国内第Ⅲ相臨床試験開始 |
| 2022年3月 | DW-1001の国内第Ⅰ相臨床試験開始 |
| 2022年8月 | K-321の米国第Ⅲ相臨床試験開始 |
| 2022年12月 | グラアルファ®配合点眼液の国内上市 H-1337の米国後期第Ⅱ相臨床試験開始 |
デ・ウエスタン・セラピテクス研究所の子会社
| 名称 | 事業内容 |
|---|---|
| (連結子会社) 日本革新創薬株式会社 | 創薬事業 |
デ・ウエスタン・セラピテクス研究所の類似企業
| 企業名 | 平均年収 | 従業員数 |
|---|---|---|
| カルナバイオサイエンス | 708万円 | 62人 |
| LTTバイオファーマ | 611万円 | 14人 |
| ジーエヌアイグループ | 1122万円 | 9人 |
| ラクオリア創薬 | 703万円 | 62人 |
| そーせいグループ | 1345万円 | 32人 |
| シンバイオ製薬 | 1208万円 | 118人 |
| キャンバス | 642万円 | 11人 |
| キッズウェル・バイオ | 737万円 | 41人 |
| ソレイジア・ファーマ | 1310万円 | 21人 |
| ナノキャリア | 708万円 | 17人 |
