綜合臨床ホールディングスの平均年収
綜合臨床ホールディングスとは
| 企業名 | 綜合臨床ホールディングス |
|---|---|
| 本社所在地 | 新宿区西新宿二丁目4番1号 |
| 売上高 | 12.4億円 |
| 社員数 | 37人 |
| 平均年収 | 609万円 |
| 推定初任給 | 27万円 |
| 年収偏差値 | 57.1 |
| 平均年齢 | 40.6歳 |
| 平均勤続年数 | 7.3年 |
有価証券報告書によると綜合臨床ホールディングスの事業内容は次の通りです。
(1) 当社の事業内容について
当連結会計年度末の当社グループは、当社(株式会社綜合臨床ホールディングス)と子会社4社(株式会社綜合臨床サイエンス、株式会社あすも臨床薬理研究所、株式会社綜合臨床メデフィ、株式会社ジェービーエス)により構成されております。
なお、当社は特定上場会社等に該当し、インサイダー取引規制の重要事実の軽微基準のうち、上場会社の規模との対比で定められる数値基準については連結ベースの計数に基づいて判断することとなります。
当社グループの事業に係る位置付け及び事業の種類別セグメントとの関連は次のとおりであります。
区分 | 会社名 | 事業内容 | 摘要 |
SMO事業 | 株式会社綜合臨床サイエンス | CRC業務、IRB事務局業務、 | 連結子会社 |
株式会社あすも臨床薬理研究所 | CRC業務、IRB事務局業務、 | 連結子会社 | |
株式会社ジェービーエス | CRC業務、IRB事務局業務、 | 連結子会社 | |
その他の事業 | 株式会社綜合臨床メデフィ | CRO事業 | 連結子会社 |
株式会社綜合臨床サイエンス | 心理評価業務 | 連結子会社 |
事業の系統図は次のとおりであります。
当社グループのコア事業であるSMO(※1)事業について
当社グループは、臨床試験(以下、治験という。)(※2)を実施する医療機関から、治験の実施に係る業務の一部を受託または代行するSMOをコア事業として、主に医療機関への支援サービスを提供しております。
一般に、医薬品の開発にあたっては、前臨床試験(※3)において、様々な方法でその安全性と有効性が試されますが、最終段階においては、被験者(※4)を対象とした治験が不可欠となります。当社は、これら治験を実施する医療機関に対し、CRC(※5)業務、IRB(※6)事務局業務及び治験事務局業務の包括的支援サービスを提供することで、治験が適正かつ円滑に実施されるように医療機関の業務を支援しております。
それぞれの業務内容は、以下のとおりであります。
CRC業務 |
CRCは、治験責任医師(※7)の指導の下、インフォームド・コンセント(※8)の取得補助、症例報告書(※9)への転記・管理、モニター(※10)との対応窓口等、医学的判断を伴わない治験業務の支援を行います。医薬品の治験実施過程において、とりわけ被験者と治験との調整を行い、治験の倫理性、科学性を保証するための活動を行います。 |
IRB事務局業務 |
製薬企業等から依頼を受けた医療機関は、IRBを開催し、倫理的、科学的及び医学的妥当性の観点から治験実施の適否を判断する必要がありますが、当社は、IRB開催の通知、資料の配布、IRB議事録の作成及び審査結果の報告等、その整備・運営に関する支援を行います。 |
治験事務局業務 |
医療機関が治験を実施するにあたり必要となる標準業務手順書(SOP)(※11)や各種書類の作成等、治験事務局の整備・運営に関する支援を行います。 |
(2) 医薬品開発の流れと当社の業務との関係について
製薬企業等では、下記に示す開発プロセスに準じ、新医薬品の開発を行っております。一般に、研究開始から製造承認の取得まで、約500億円に及ぶ研究開発費と10~17年もの長い歳月が必要と言われております。
当社は、下記の開発プロセスの中で、医療機関における臨床試験(治験)及び市販後調査に関する事務的な業務を受託または代行しております。
また、当社は、医療機関が、GCP省令(※12)に準拠した適正な治験を実施するためのインフラ整備を支援するとともに、治験を実施しようとする医療機関と治験を依頼する製薬企業等とのマッチングサービスを行うなど、包括的な業務を提供しております。
具体的な医薬品開発及び当社の業務の流れは、以下のとおりであります。
製薬企業は、治験の運営と管理に係わる業務の一部または全部を行うCRO(Contract Research Organization:開発業務受託機関)(※13)を起用する場合があります。
CROは製薬企業の業務を受託し、一方、SMOは実施医療機関の業務の一部を受託または代行するものでありますが、製薬企業等と実施医療機関に「なれあい」が生じる可能性が考えられ、このようなことは治験データの信頼性の確保の観点から好ましくないため、CROとSMOは治験の実施にあたり、相互に独立性を確保する必要があります。
当社の委受託の関係図は以下のとおりであります。
(3) 我が国におけるSMOの位置付けについて
SMOは、1970年代に米国において治験責任医師が治験業務の効率化を図るため、治験に係る事務的な業務等を外部に委託したことから始まっております。
我が国においては、平成元年10月に通知された厚生省薬務局通知「医薬品の臨床試験の実施に関する基準について」(以下、「旧GCP(※14)」という。)に基づいて、大学病院等を中心に治験が実施されておりました。
平成9年に旧GCPの大幅な改正が行われ、新たにGCP省令が施行されました。GCP省令の施行後、医療機関における治験実施体制のより充実した整備等が求められるようになり、治験に関する事務的な業務等も増加いたしました。
平成15年6月にはGCP省令が改正され、SMOが行う業務の取り扱いが法令上正式に規定されました(厚生労働省令第106号)。同省令の第39条の2の規定で、「実施医療機関は、治験の実施に係る業務の一部を委託する場合には、次に掲げる事項を記載した文書により当該業務を受託する者との契約を締結しなければならない。」と記載されております。
製薬企業等が推進する医薬品開発については、引き続き高齢化社会に対応した生活習慣病向けの新医薬品開発が主でありますが、昨今では患者から強い要望があるにも関わらず、有効な治療法が少ない医療ニーズに対して開発を強化する製薬企業も増えてきております。このような治療の対象となる患者は、小規模病院ではなく大規模病院を利用する傾向があり、従来の小規模医療機関中心のSMOによるサービス提供に加え、大規模病院等へ対応していく必要性が見込まれております。
また、平成24年3月には「臨床研究・治験活性化5か年計画2012」が文部科学省・厚生労働省から公表され、革新的な医薬品創出に向けた体制の強化や、開発が進みにくい分野への取り組み強化等を課題としております。
近年、SMO市場におきましては、ドラッグ・ラグの解消を目指した治験の早期化ニーズや国際共同治験の増加に伴って、コストの安さや医療機関と製薬企業との調整といった従来からの要求に加え、少数の施設で多くの被験者を集め効率的に治験を実施することや、アンメット・メディカル・ニーズを満たすニッチ領域の被験者を集めることができる提携医療機関の診療領域の豊富さ、大型治験の実施に際しても全国一律に対応することができる品質等が求められるようになってまいりました。
(用語説明)
※1 SMO(Site Management Organization:治験施設支援機関)
治験(※2)を実施する医療機関から、治験の実施に係る業務の一部を受託または代行する組織。
※2 臨床試験(治験)
医薬品開発のプロセスにおいて、人を対象として、薬の安全性や有効性を確認するための試験。
特に、臨床試験のうち、医薬品の製造(輸入)承認または承認事項の一部変更承認を申請する際に提出すべき資料の収集を目的として実施される試験を治験という。
※3 前臨床試験
動物を用いて安全性、有効性等を検討するための試験。非臨床試験ともいう。
※4 被験者
治験に参加し、治験薬を投与される者またはその対象となる者。
※5 CRC(Clinical Research Coordinator:治験コーディネーター)
質の高い治験を適正かつ円滑に進めるために、治験責任医師(※7)の指導のもと、医学的判断を伴わない治験業務(インフォームド・コンセント(※8)の取得補助、被験者のケア、治験に携わるチーム内の調整業務等)の支援を行う者。
※6 IRB(Institutional Review Board:治験審査委員会)
医療機関の長、治験責任医師及び製薬企業等から独立した医学・薬学等の専門家及びそれ以外の者によって構成される委員会。当委員会の責務は、治験実施計画書(※15)や被験者から文書によるインフォームド・コンセントを取得するための手法及び資料等を審査し、被験者の人権、安全及び福祉の保護を確保することである。
※7 治験責任医師
医療機関において、治験の実施に関して責任を有し、治験に係る業務を統括する医師または歯科医師。
※8 インフォームド・コンセント
被験者の治験への参加を決定する際に、治験に関するあらゆる角度からの説明が充分なされた後に、被験者がこれを理解し、自由な意思によって治験への参加に同意し、書面によってそのことを確認すること。インフォームド・コンセントは、被験者と担当医師による署名と日付が記入された同意文書をもって証明される。
※9 症例報告書
治験実施計画書において規定される、各被験者に関する全ての情報を記録するための文書。
治験責任医師若しくは治験分担医師が原資料(カルテ等)を基に作成し、製薬企業等に報告することが義務付けられている。
※10 モニター/モニタリング
製薬企業等により指名されたモニター(CRA:Clinical Research Associate)が、治験の進行状況を調査し、治験がGCP省令(※12)、治験実施計画書、標準業務手順書(※11)に従って実施、記録及び報告されていることを保証する活動。
※11 標準業務手順書(SOP:Standard Operating Procedures)
治験に係る業務を均質に遂行するための手順を詳細に記述した文書。
※12 GCP省令(Good Clinical Practice)
平成9年厚生省令第28号「医薬品の臨床試験の実施の基準に関する省令」。治験が倫理的な配慮のもとに科学的に適正に実施されるための基準である。
※13 CRO(Contract Research Organization:開発業務受託機関)
医薬品の開発において、製薬企業等の治験に係わる業務の一部を受託または代行する個人または組織・団体。
主な業務内容として、治験の依頼業務、モニタリング(※10)・監査(※16)、データマネジメント・統計解析、製造承認申請等がある。
※14 旧GCP(Good Clinical Practice)
平成元年10月2日付、薬発第874号薬務局通知「医薬品の臨床試験の実施に関する基準について」。治験が倫理的な配慮のもとに科学的に適正に実施されるための基準である。
※15 治験実施計画書(プロトコール)
治験の目的、デザイン、方法等について記述した文書。治験を実施するにあたって、医療機関及び製薬企業等が遵守しなければならない要件事項を記載した実施計画書である。
※16 監査
治験により収集されたデータの信頼性を確保するため、治験がGCP省令、治験実施計画書、標準業務手順書に従って実施されているか否かについて、製薬企業等によって指名された監査担当者が、独立の立場から検証を行う。
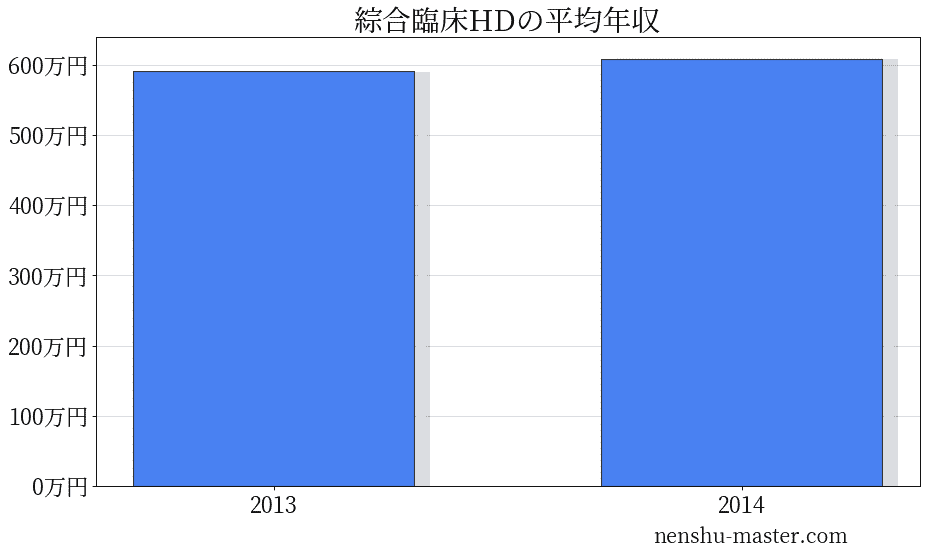
綜合臨床ホールディングスの平均年収は609万円
生涯収入の全国平均である約1.9億円に対し、綜合臨床ホールディングスの生涯収入はおよそ2.25億円と推定されます。
| 年 | 平均年収 |
|---|---|
| 2013 | 591万円 |
| 2014 | 609万円 |
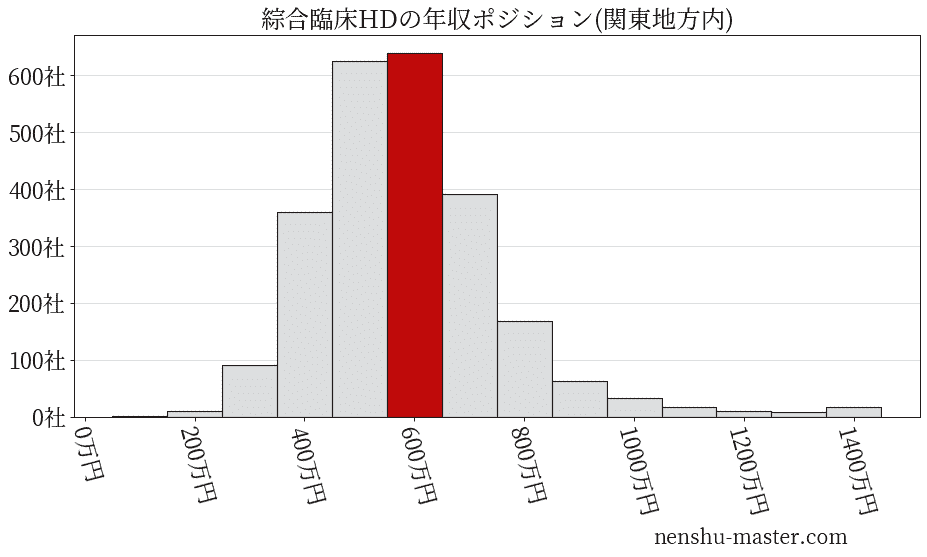
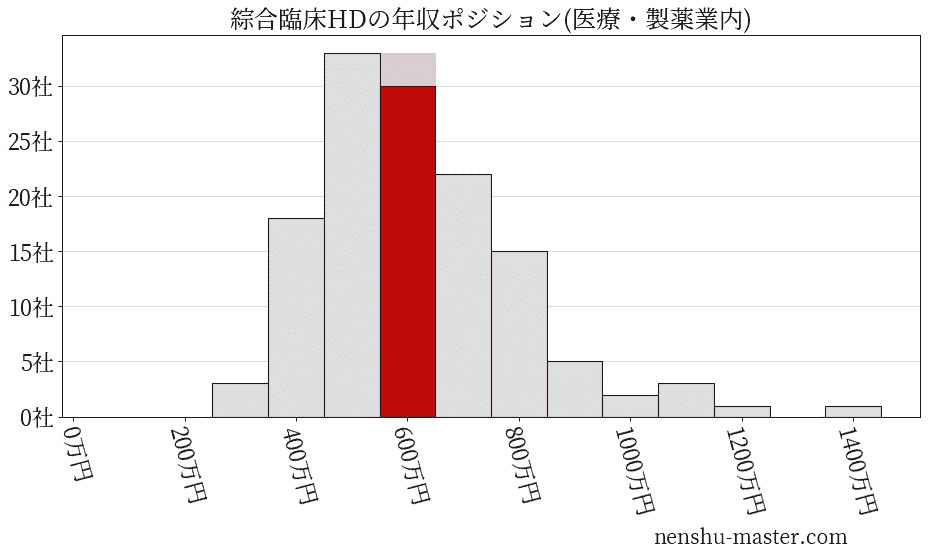
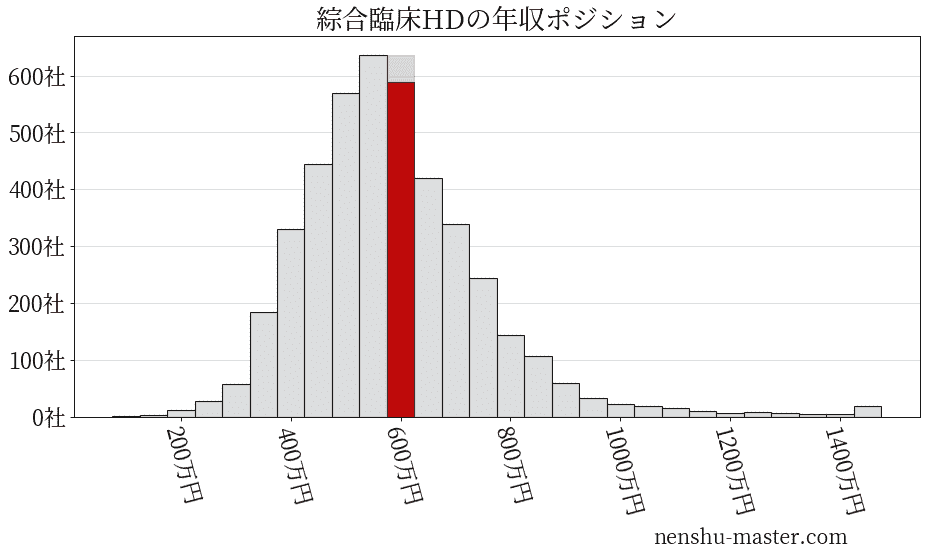
平均年収と社数のヒストグラム上では綜合臨床ホールディングスは赤色の箇所に位置しています。 年収ランキングでは綜合臨床ホールディングスは2249位(全4687社)で、年収偏差値は57.1でした。
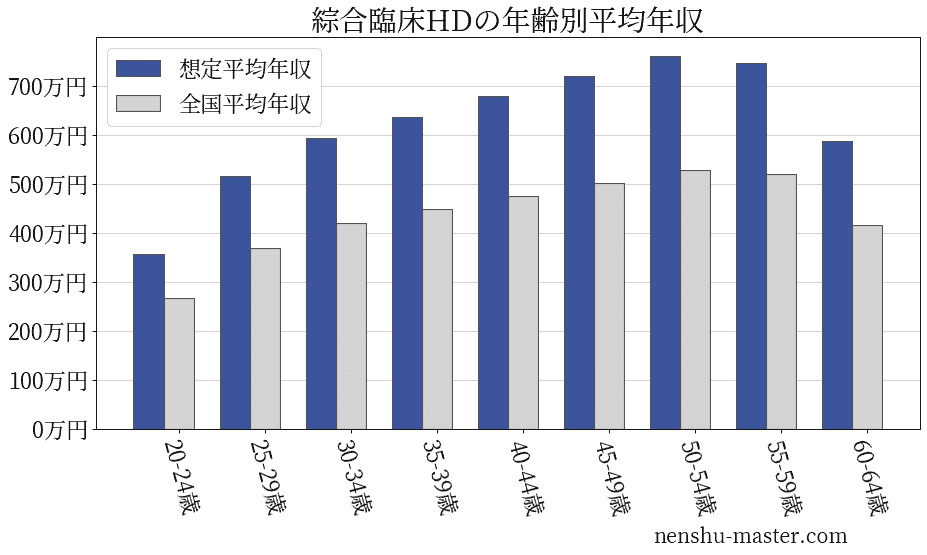
綜合臨床ホールディングスの年齢別年収
| 年齢 | 想定平均年収 | 月額給与 |
|---|---|---|
| 20-24歳 | 357万円 | 27万円 |
| 25-29歳 | 516万円 | 40万円 |
| 30-34歳 | 593万円 | 46万円 |
| 35-39歳 | 637万円 | 49万円 |
| 40-44歳 | 680万円 | 52万円 |
| 45-49歳 | 720万円 | 55万円 |
| 50-54歳 | 762万円 | 59万円 |
| 55-59歳 | 748万円 | 58万円 |
| 60-64歳 | 587万円 | 45万円 |
綜合臨床ホールディングスの賞与・ボーナス
| 年 | 平均賞与額 |
|---|---|
| 2013 | 24万円 |
| 2014 | 26万円 |
綜合臨床ホールディングスの業種・地域
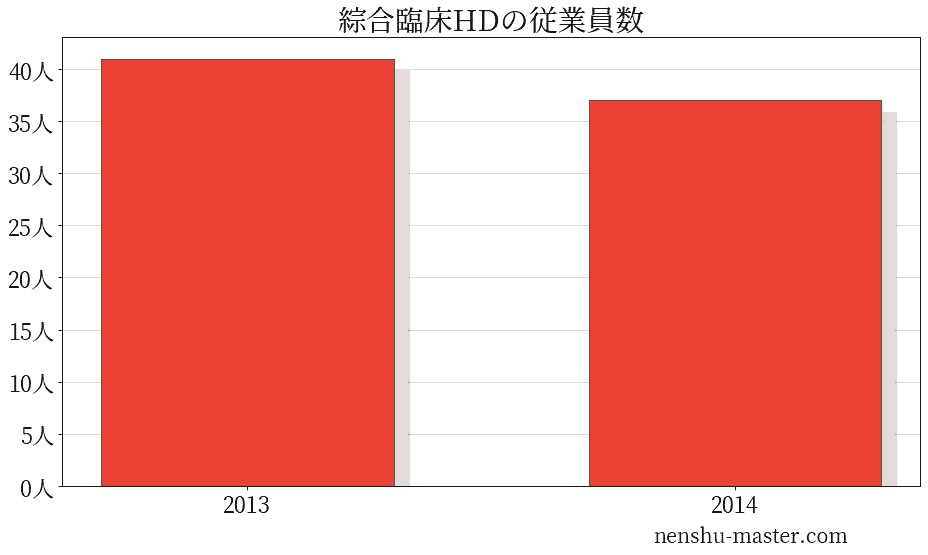
綜合臨床ホールディングスの従業員数は37人
| 年 | 従業員数 |
|---|---|
| 2013 | 41人 |
| 2014 | 37人 |
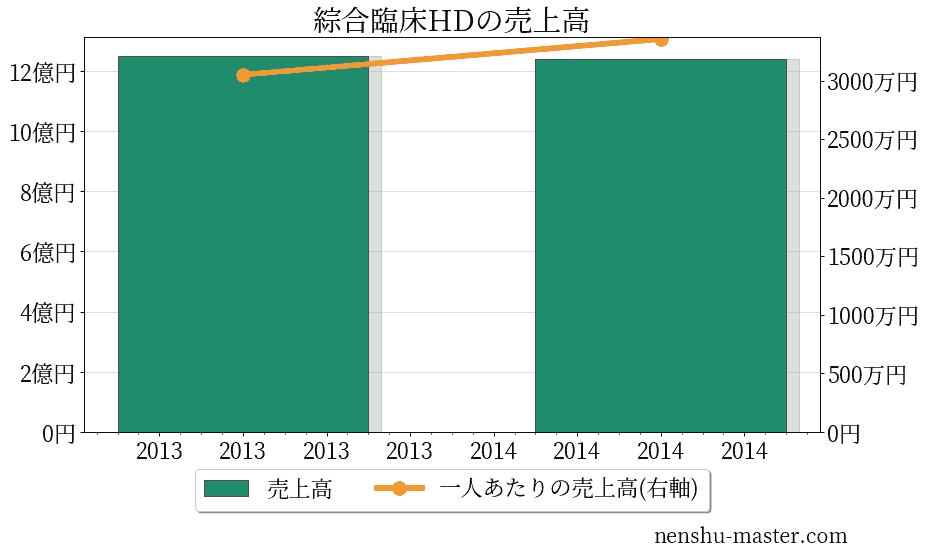
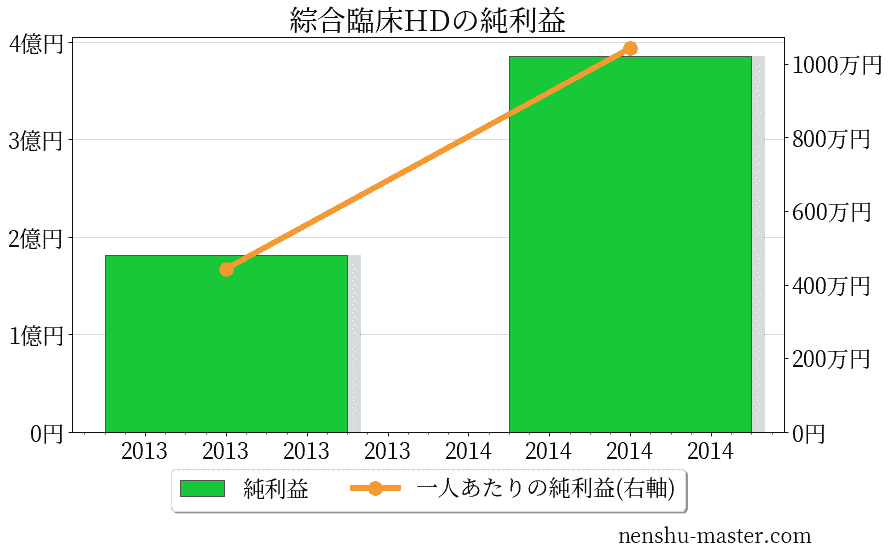
綜合臨床ホールディングスの売上、純利益
【広告】綜合臨床ホールディングスに転職するには?
転職サイトはサイトごとに特色があり、2〜3サイトを登録してそれぞれの良い部分を利用するのが賢い利用方法です。年収マスターイチオシのサイトを紹介します。
JACリクルートメント
「JACリクルートメント」はハイクラスな転職案件を多数持っており、市場価値の高い応募者におすすめのサイトです。 内資系の高額案件はもちろん、JACリクルートメントはイギリスやシンガポールでも展開しており、そのつながりを活かした外資系案件も多数あります。
他の転職サイトでは一気に大量の案件を提示されることがありどれを選べばわからないということが起こりますが、JACリクルートメントではそのようなことはありません。 ひとりの応募者につき複数のエージェントが担当し、選りすぐりの案件を紹介してくれるためマッチ度が高い仕事に出会えます。
ハイクラス案件をメインで扱うJACリクルートメントのみでしか得られない案件情報も多数あります。 上昇志向があり、現在のポジションからステップアップしてよりハイキャリアを目指す方にはイチオシのサイトです。
ランスタッド
「ランスタッド」は敏腕コンサルタントが専任で案件紹介をしてくれる転職サイトです。 ランスタッドのエージェントは評判が良く、最近人気が大きく伸びてきてきています。 よくある転職サイトはエージェントが十分なヒアリングも無くノルマ達成のためにたくさんの案件を紹介してきますが、 ランスタッドはそのようなことはありません。
ランスタッドは少数精鋭のコンサルタントで運営されており、現状のスキルや今後構築したいキャリアなどを入念にヒアリングした上で案件紹介をしてくれます。 特に20代後半から30代の転職に力を入れており、応募者にマッチした案件を紹介してくれます。
そのため案件の質も高く、JACリクルートメントと同様に高年収案件に強い印象です。800万円や1200万円を超える案件も多数あり、 ハイキャリアを目指す方には心強いパートナーです。ランスタッドのみでしか公開されてない案件もかなり多いので、 一度無料登録して相談してみることをオススメします。
参考書籍
綜合臨床ホールディングスの歴史
| 平成元年12月 | 臨床試験実施の支援を目的として、東京都八王子市新町に資本金500万円で株式会社綜合臨床薬理研究所を設立。 |
| 平成2年8月 | エヌ・エスクリニックと業務提携し、第Ⅰ相試験(注1)のCRC業務(注2)を開始。 |
| 平成5年10月 | 第Ⅱ相試験(注1)のCRC業務を開始。 |
| 平成10年2月 | 第Ⅲ相試験(注1)のCRC業務を開始。 |
| 平成11年7月 | 第Ⅳ相試験(注1)のCRC業務を開始。 |
| 平成16年4月 | 株式会社東京証券取引所マザーズ市場に株式を上場。 |
| 平成24年2月 | SOGO学術委員会を設置。 |
| 平成24年4月 | 株式会社綜合臨床メデフィを当社100%出資会社として設立。 |
| 平成25年7月 | 株式会社東京証券取引所市場第一部へ上場市場を変更。 |
| 平成27年9月 | 株式会社綜合臨床エムケアを当社100%出資会社として設立。 |
綜合臨床ホールディングスの子会社
| 名称 | 事業内容 |
|---|---|
| (連結子会社)株式会社綜合臨床サイエンス | SMO事業その他の事業(心理評価業務) |
| (連結子会社)株式会社あすも臨床薬理研究所 | SMO事業 |
| (連結子会社)株式会社綜合臨床メデフィ | その他の事業(CRO事業) |
| (連結子会社)株式会社ジェービーエス | SMO事業 |
綜合臨床ホールディングスの類似企業
綜合臨床ホールディングスと平均年収が近い企業
| 企業名 | 平均年収 |
|---|---|
| オルバヘルスケアHD | 609万円 |
| ソフトマックス | 532万円 |
| エス・ディー・エス バイオテック | 677万円 |
| グラフィコ | 541万円 |
| 扶桑薬品工業 | 553万円 |
| 富士製薬工業 | 667万円 |
| 森田薬品工業 | 499万円 |
| データホライゾン | 495万円 |
| 日本アイ・エス・ケイ | 508万円 |
| マニー | 614万円 |